核酸DDS:遺伝子を標的にした治療を実現する薬物送達技術 ~特許・論文・グラントの研究開発動向分析~
著者:アスタミューゼ株式会社 平澤 輝一 博士(理学)
目次
核酸DDSとは
核酸DDS(ドラッグデリバリーシステム)とは、siRNA(小分子干渉RNA)やASO(アンチセンス核酸)、mRNA(メッセンジャーRNA)などの核酸医薬を、標的細胞の内部まで安全かつ効率的に送達するための技術体系を指します。
核酸医薬は、遺伝子のはたらきをそのおおもとから調節できる次世代の治療手段です。薬を体内の目的の細胞までとどけるしくみ(核酸DDS)には、脂質ナノ粒子(LNP)とよばれる超微細な脂質の粒がつかわれています。LNPは細胞の表面に付着したのち、細胞にとりこまれ「エンドソーム」とよばれる細胞内の小さな袋のなかにとじこめられます。
この核酸(薬の本体)がその効果を発揮するには、この袋をやぶって脱出し、細胞内の作用場所にたどりつかねばなりません。袋をやぶるためには、エンドソームのマイナスに帯電した膜に働きかけて膜をこわす必要があります。しかし従来のLNPは、エンドソーム内の酸性環境でプラスの電荷を十分に帯びることができず、膜を効果的にこわせないという問題がありました。
また、核酸は体内に存在する分解酵素(ヌクレアーゼ)によって壊されやすく、マイナス電荷を持つため細胞膜を通り抜けにくいという難点もあります。
最新の核酸DDS開発ではこれら複数の課題を克服し、核酸医薬の効果を最大限に引きだすことがこころみられています。
次世代の核酸DDSが従来と大きくことなるのは、薬を目的の細胞に「とどける」だけではなく、細胞の内部で薬が実際にはたらく場所まで確実に「送りこむ」ことを目指している点です。
こうした技術はすでに実用段階に入っており、新型コロナウイルスの mRNAワクチンや遺伝性疾患の治療薬への応用を通じて、その有効性が世界規模で実証されています。
次世代型だけではなく従来型もふくんだ、おもな核酸DDS技術とその特長は以下となります。
- 脂質ナノ粒子(LNP、従来型~次世代型):mRNAやsiRNAを脂質でつつみこみ、生体内での分解から核酸を保護しつつ標的細胞へ送達する
- アクティブターゲティング(次世代型):目印となる分子(抗体・糖鎖リガンド)をあらかじめ付与しておくことで、がん細胞など狙った組織に選択的に薬をとどける
- コンジュゲート型DDS(従来型~次世代型):薬の本体である核酸に、細胞への結合をたすける特定の分子(糖鎖やペプチド、抗体等)を直接結合させることで「運び屋」となる粒子を別途必要とせずに、狙った細胞へ効率的に取り込まれるようにする手法であり、改良と進化が続いている技術。
- 修飾核酸技術との併用:核酸そのものの化学構造に手を加える(ホスホロチオエート化、2′-O-メチル修飾、2′-フルオロ修飾等)ことで、体内での分解を受けにくくし、薬の効果をながく持続させる技術。DDSと組み合わせ以前から活用されてきた手法。
- エンドソーム脱出機能(従来型~次世代型):細胞に取り込まれた薬が、細胞内の「袋」に閉じ込められたままにならないよう、その袋を内側から破り、薬が実際にはたらく場所へたどりつけるようにする機能。イオン化脂質が酸性環境でカチオン化しエンドソーム膜を破壊、核酸を細胞質に放出する。長年にわたり改良が重ねられてきた。
- 多様な治療手段への対応(次世代型):遺伝子の発現をおさえる、修復する、あるいは免疫を活性化するなど、異なる作用メカニズムをもつ幅広い種類の核酸医薬(siRNA、ASO、mRNA、miRNA、CpGオリゴヌクレオチド等)に対応できる汎用性の高さが特徴。
このレポートでは、アスタミューゼ独自のデータベースを活用し、特許と論文、グラント(競争的研究資金)における「核酸DDS」に関連する技術動向を分析しました。
核酸DDSに関連する特許の動向
アスタミューゼの保有する特許データベースから、「脂質ナノ粒子」、「mRNAデリバリー」、「核酸医薬」など、核酸DDSに関連する技術キーワードを要約にふくむ特許母集団2,256件を抽出し、キーワードの年次推移から近年進展のある技術要素を特定する「未来推定」分析を実施しました。キーワードの変遷を把握することで、現在または将来的に脚光をあびると予測される技術を定量的に評価できます。
図1は、2015 年以降に出願された核酸DDS関連特許のキーワード年次推移です。
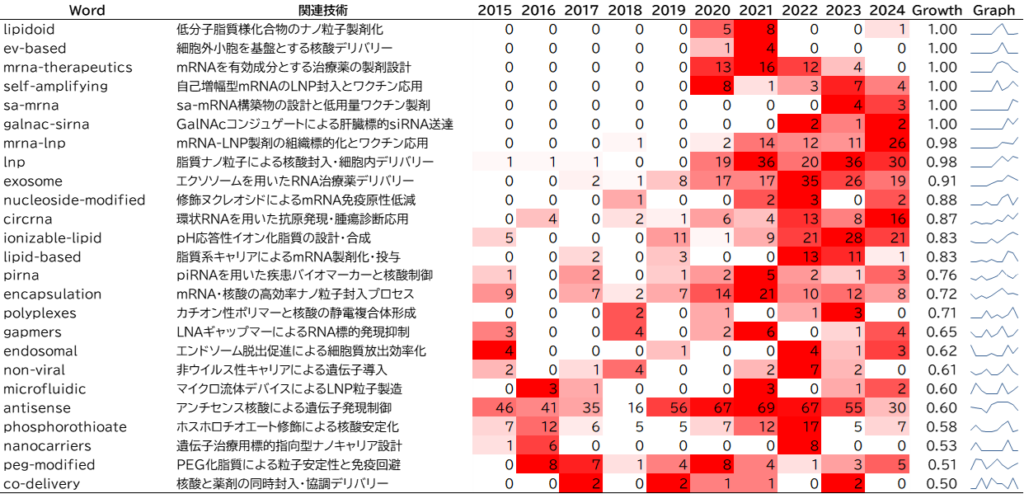
Growthは、2015年から2024年までの出現回数と、2020 年以降の出現回数の比です。値が1に近いキーワードほど直近の出現頻度が高く、近年注目されているキーワードとみなせます。
Growth上位には「ナノ粒子製剤化」、「ワクチン」、「RNA製剤の送達」に関するキーワードが多くなっています。とくに注目のキーワードを紹介します。
- lipidoid(脂質様物質):mRNAおよびsiRNAの送達用ナノ粒子の製造に利用される。従来の天然脂質や非特異的ウイルスベクターとことなり、化学的に設計された脂質様構造体が核酸を効率的に細胞内へ導入。核酸医薬の細胞内送達基盤の中核をになうことが期待される。
- sa-mrna(自己増幅型mRNA):ウイルス由来のRNA複製機構を搭載したmRNAによるワクチンおよび治療技術のキーワード。通常のmRNAワクチンにくらべると、細胞内で転写産物が自律的に増幅するため、ごく少量の投与量で効果がある。新型コロナウイルス対応ワクチンの研究でも利用される一方、感染症以外の疾患領域にも展開が期待される次世代治療技術。
- galnac-sirna(N-アセチルガラクトサミン修飾siRNA):siRNA (遺伝子の発現を押さえる核酸医薬)に、肝細胞の表面にある特定の受容体と結合しやすい分子(GalNAc)をあらかじめ付与することで、薬を肝臓に選択的にとどける技術。肝細胞への結合精度が非常に高いため、他の組織への影響をおさえながら、肝臓内の特定の遺伝子のはたらきを効率よく抑制できる。従来の薬のようにタンパク質を標的とするのではなく、遺伝子の発現そのものにはたらきかけるのが特徴で、を肝疾患の治療における有力な選択肢として注目されている。
これらのキーワードの急伸は、LNP素材の多様化や次世代mRNA治療技術の台頭、標的送達の実用化加速を反映しています。
以下に、「lipidoid(脂質様物質)」と「sa-mrna(自己増幅型mRNA)」に関する特許事例を紹介します。
- 細胞内mRNA送達のためのpH応答性リピドイドナノ粒子
- 公報番号:US20230321036A1
- 公開年:2023年
- 機関/企業:Trustees of Tufts College
- 国:アメリカ
- 概要:細胞内の環境変化に反応して薬を放出する新しい設計の脂質ナノ粒子(R-O16CBA LNP)。薬を包む粒子に特殊な化学構造を組みこむことで、細胞に取りこまれた後、細胞内の酸性環境をトリガーとして粒子が自律的に崩壊し、内包するmRNAを効率よく放出する仕組みを実現した。細胞への毒性を大幅におさえながら高い送達効率を両立しておりがん治療や感染症向けのmRNA医薬を安全に細胞内へとどける技術として応用が期待される。
- 分泌抗原および免疫調節物質を含む合成自己増幅型mRNA分子
- 公報番号:CN119563028A
- 公開年:2025年
- 機関/企業:SHANGWEI TIANCHENG XINSHI NUCLEIC ACID THERAPY
- 国:中国
- 概要:あたらしい自己増幅型mRNA(sa-mRNA:細胞内で自分自身をコピーして増殖できるmRNA)の構築体を開発。新型コロナウイルスのスパイクタンパク質を改良(細胞膜に結合しない分泌型に改変)したものと、免疫反応を調節する因子(IL12、IL21等)を同時に作らせる設計になっている。また、あたらしく開発したイオン化脂質E6などをもちいた脂質ナノ粒子製剤により、細胞への毒性をおさえながら高い遺伝子導入効率を実現した。
つづいて、特許出願数の国別動向です。企業や研究機関の出願する特許の傾向には、社会実装が近い、あるいはすでに実装済みである技術と関連する短中期の動向が反映されます。
核酸DDSに関連する特許の国別出願件数の年次推移が図2です。なお、特許データは出願から公開までにタイムラグが存在するため、2023年までの集計値となっています。
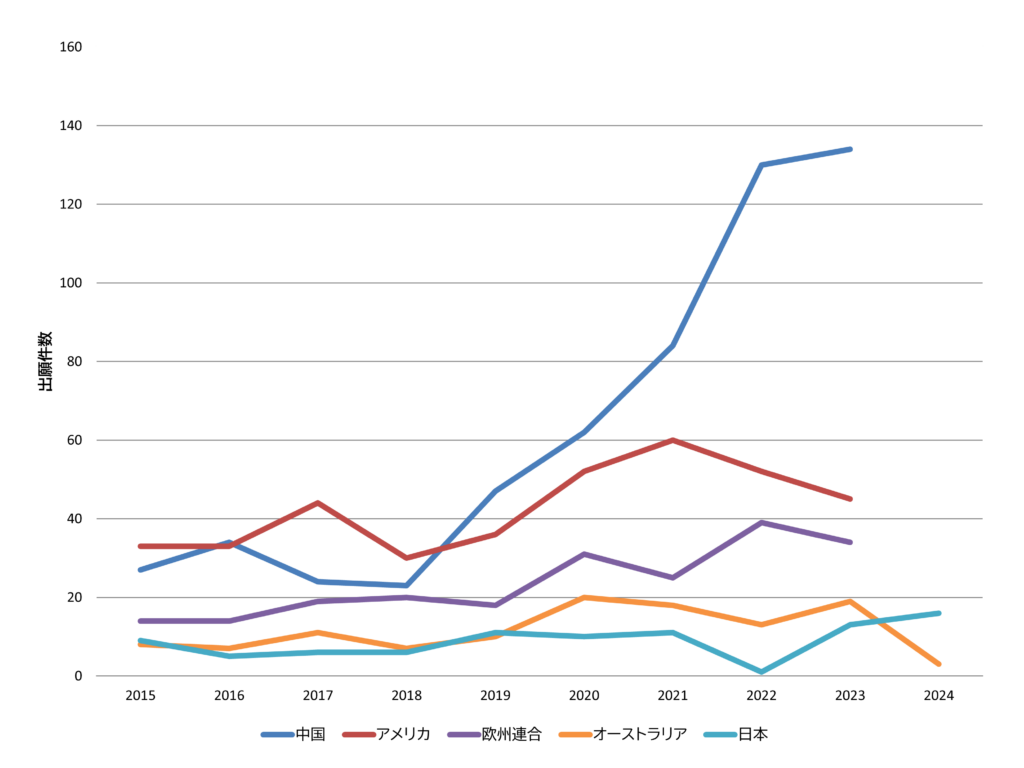
特許出願数では、中国の特許出願の伸びが目立ちます。つづいて、アメリカや欧州も多くの出願をおこなっています。
中国ではGUANGZHOU GUSEN PHARMACEUTICALやJIACHEN XIHAI (HANGZHOU) BIOTECHNOLOGYといった製薬バイオベンチャー企業を中心に、イオン化脂質(薬をつつむ脂質粒子の材料)の開発とその製剤化技術(LNP製剤化)に関する特許出願が集中しており、核酸DDSの基盤となる材料分野での特許戦略が活発化していることがうかがえます。
核酸DDSに関連する論文の動向分析
企業や研究機関から発表される論文は、研究開発段階にあり、特許と比較すると社会実装までに時間のかかる技術の中長期的動向を反映します。
特許分析と同様に、核酸DDSに関連する特徴的なキーワードをふくむ論文母集団15,638件を抽出しました。2015 年以降に出版された核酸DDSに関連する論文の概要に含まれるキーワードの年次推移が図3です。
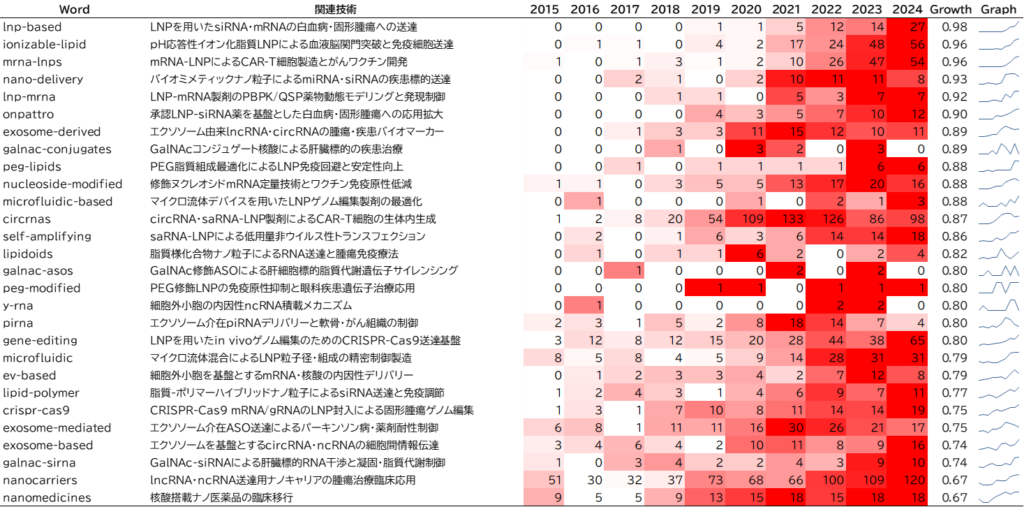
2015年以降の論文で増加傾向にあるキーワードは以下となります。
- onpattro(RNA干渉[RNAi]治療薬の1種):世界で初めて承認されたsiRNA医薬品で、脂質ナノ粒子(LNP)をもちいて肝臓に薬をとどける製剤。LNPにつつまれたsiRNAが肝細胞に取りこまれると、トランスサイレチン遺伝子のはたらきを抑制し、遺伝性アミロイドーシス(異常なタンパク質が体内に蓄積する遺伝病)を治療する。脂質ナノ粒子を使った核酸医薬の臨床実証例として頻繁に参照され、後に続く薬の設計における基準点となっている。
- peg-lipids(ポリエチレングリコール結合脂質):脂質ナノ粒子(LNP)の表面をおおって、薬のはたらきを改善するための脂質成分。量子の表面にPEG鎖という親水性の分子を配置することで、粒子同士がくっついて塊になることを防ぎ、血液中での安定性を高め、免疫系による攻撃を回避させる効果がある。これによりmRNAやsiRNAが体内でより効率的に作業できるよう制御する。mRNAワクチンや治療薬のLNP製剤の最適化研究が急増する中、、構成材料の設計を論じる研究文献で広く言及される成分。
- nucleoside-modified(修飾ヌクレオシド):免疫反応を避けつつmRNAの構成要素である塩基を人工的に改変する技術。mRNA(ウリジン)を改良した塩基(シュードウリジン等)におきかえることで、体の免疫システムに異物として認識されることを回避しつつ、目的とするタンパク質をより多く作らせることができる。新型コロナウイルスのmRNAワクチンの成功により、この技術の有効性が実証されたことで、感染症以外のさまざまな病気を対象とした治療用mRNAの研究開発が急速に拡大している。
- microfluidic(マイクロ流体):マイクロメートル単位の微細な管を使って脂質ナノ粒子(LNP)を製造する技術。薬をつつむ脂質、核酸、その他の添加剤を微細な流路の中で精密に混合することで、粒子のサイズや薬の封入率、品質の均一性を高精度で制御したLNPを、毎回安定して製造できる。核酸医薬の大量生産への需要が高まる中、LNP製剤開発における標準的な製造手法として、関連する研究報告が急速に増加している。
- exosome-mediated(エクソソーム介在):細胞が自然に分泌する小さなカプセル(エクソソーム)を利用して、遺伝子情報やタンパク質を細胞感でやりとりする現象。エクソソームが特定の核酸(lncRNAやmiRNAなど)を包みこんで目標の細胞に取り込まれることで、がんの増殖や転移、免疫反応の調節といった重要な生物学的プロセスに関与するメカニズム。もともと体内に存在する天然由来のカプセルであるため免疫反応を起こしにくく、人工的な脂質ナノ粒子(LNP)に代わるあたらしい核酸送達手段として注目が集まっている。
これらのキーワードからわかるように、核酸DDS分野の論文では、製剤設計や塩基修飾、製造技術、生体由来担体に関して革新が進み、有効性・安全性・製造基盤を総合的に底上げしています。とくに、装飾ヌクレオシド技術により改良されたmRNAの治療応用拡大と微細流路技術(マイクロ流体)による脂質ナノ粒子(LNP)の製造標準化が主要トレンドです。
以下に、注目の論文事例を紹介します。
- Predictive high-throughput screening of PEGylated lipids in oligonucleotide-loaded lipid nanoparticles for neuronal gene silencing(神経細胞遺伝子サイレンシングのためのオリゴヌクレオチド搭載脂質ナノ粒子中のPEG化脂質の予測的ハイスループットスクリーニング)
- 雑誌名:Nanoscale advances
- 出版年:2022年
- DOI:https://doi.org/10.1039/D1NA00712B
- 機関名:Genentech Inc.(アメリカ)、ローレンス・バークレー国立研究所(アメリカ)、カリフォルニア大学サンタクルーズ校(アメリカ)
- 概要:54種類のASO-LNP製剤(遺伝子発現抑制薬をつつんだ脂質ナノ粒子)を自動化装置で効果を比較検討し、表面をおおうPEG化脂質の設計要素がどのような影響をあたえるかをくわしく解析した。その結果、マイナス帯電したPEG化脂質の配合比率が粒子サイズを決定し、脂質分子の炭素鎖の長さが遺伝子抑制効果の強さを左右することを発見した。この自動化された評価システムにより、複数の設計要素を効率的に検証できるようになり、さまざまな細胞を標的とした核酸送達用脂質ナノ粒子の最適化が大幅に加速されることが期待される。
- A single vaccination of nucleoside-modified Rabies mRNA vaccine induces prolonged highly protective immune responses in mice(ヌクレオシド修飾狂犬病mRNAワクチンの1回接種による、マウスの高効率長期免疫応答の誘導)
- 雑誌名:Frontiers in immunology
- 出版年:2023年
- DOI:https://doi.org/10.3389/fimmu.2022.1099991
- 機関名:Fudan大学(中国)
- 概要:狂犬病ウイルスの表面タンパク質(RABV-G)の遺伝子情報を組みこみ、さらに装飾ヌクレオシド技術をもちいた改良型mRNAを脂質ナノ粒子でつつんだワクチンを、マウスで効果検証した。1回の接種だけで、従来の不活化ワクチンを3回接種した場合を上まわる抗体反応とT細胞免疫の両方を誘導し、低用量でも致死的ウイルス感染から動物を守ることができた。さらに、2回接種することで、すくなくとも1年間にわたった高い防御免疫が持続することが示された。
図4は、論文の国別出版件数の年次推移です。
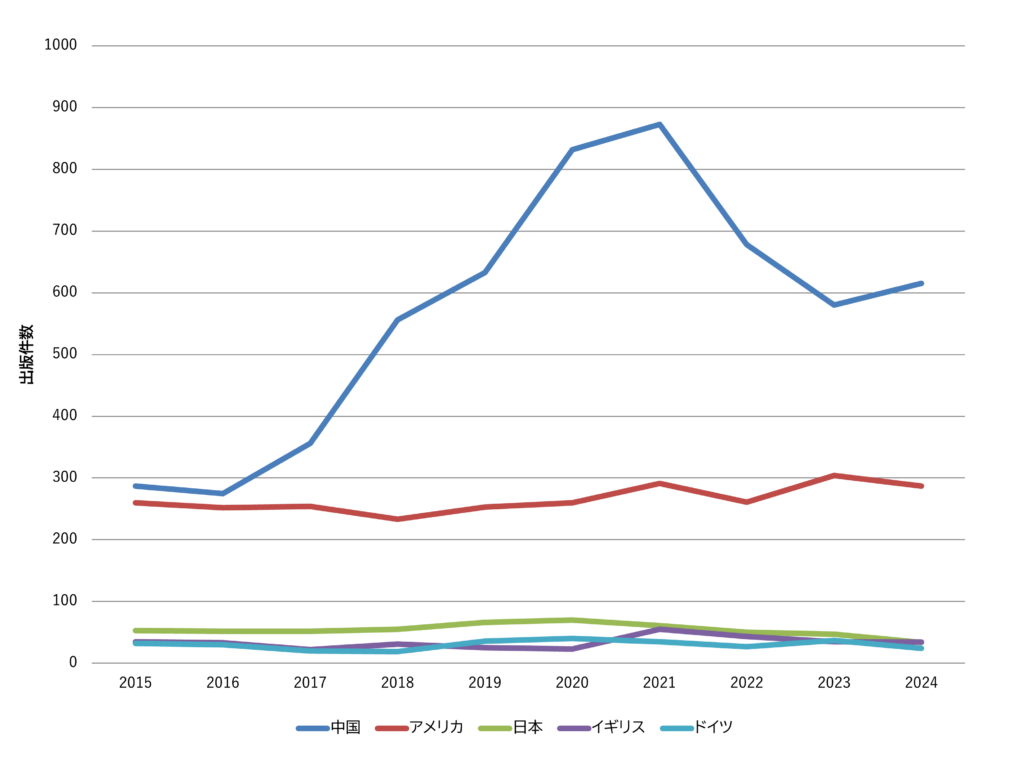
国別の論文出版件数でも、中国が突出しています。2020年ごろから急増していた特許出願件数に先行するように、2018年ごろから論文出版件数が急増しています。この時期に得られた研究成果が数年後に特許として出願され、社会実装されつつある可能性が考えられます。
核酸DDSに関連するグラント事例
つづいて、グラント(競争的研究資金)配賦額の動向分析です。企業や研究機関に賦与されるグラントは、特許や論文と比較すると社会実装にさらに長い時間が必要な研究計画段階にある技術の動向が反映されます。
特許と論文の分析と同様に、核酸DDSに関連するキーワードをふくむグラント母集団3,945件を抽出しました。2015 年以降の核酸DDSに関連するグラントの要約にふくまれるキーワードの年次推移が図5です。
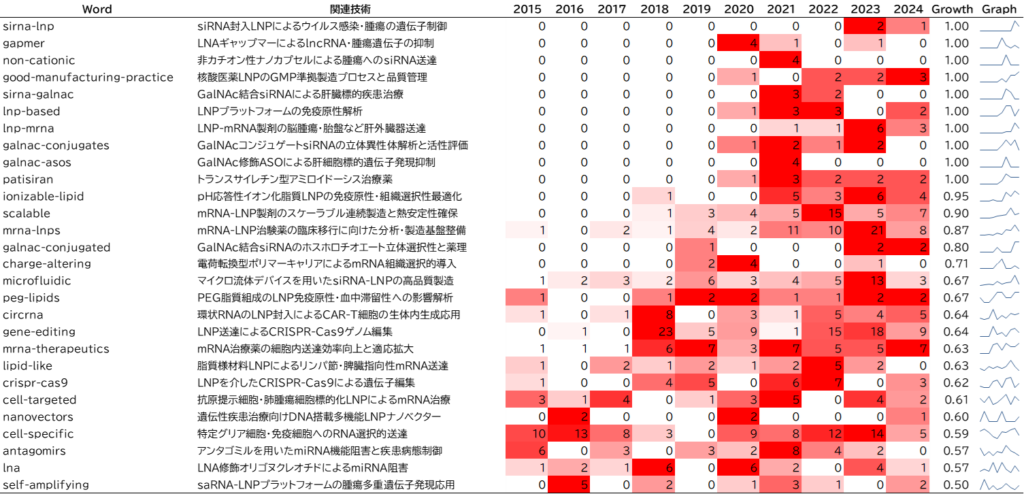
核酸DDSに関連するグラントにおける特徴的なキーワードをピックアップします。
- gapmer(ヌクレアーゼ耐性アンチセンス核酸):DNAとRNAを組みあわせた設計により、体内の分解酵素に対する抵抗性を高めたアンチセンス核酸(標的遺伝子の発現を抑制する核酸医薬)。細胞内の酵素(RNaseH)を利用して標的となるRNAを切断するしくみで、遺伝子のはたらきを効果的に止めることができる。タンパク質をつくらない遺伝子(非コードRNA)などを標的とした遺伝子発現抑制技術として、感染症や急性骨髄性白血病(AML)などの治療応用研究にグラントが集中的に投じられている。
- good-manufacturing-practice(製造管理及び品質管理の基準):核酸医薬や脂質ナノ粒子製剤の臨床応用にむけた品質保証と製造管理基準。mRNAやLNPをこの基準に適応した方法で製造するプロセスを確立し、実験室レベルから臨床試験に必要な大量生産レベルへの製造規模拡大を目指す研究開発で言及される重要な規制要件。
- scalable(大規模に実現可能):核酸医薬や脂質ナノ粒子の製造を、実験室レベルから患者向けの大量生産まで段階的に拡大できる製造プロセス設計技術。mRNA治療薬やワクチンの製造インフラを整備し、設計段階から品質を作りこむ(Quality by Design,QbD)アプローチにより、医薬品製造の幻覚な基準(GMP)に対応した製造体制の確立をめざす研究開発が活発化している。
- antagomirs(アンタゴミル):遺伝子発現を調節する小さなRNA分子(miRNA)のはたらきを、化学修飾した短いオリゴ核酸で阻害するmiRNA拮抗薬技術。乳がん、骨疾患、糖尿病性腎症、多発性硬化症など、miRNAの異常なはらたきが病気の発症や進行に関わっている疾患を対象とした治療研究が活発に進められている。
- LNA(Locked Nucleic Acid):核酸分子の構造を人工的に固定することで、標的となるRNAやmiRNAへの結合力と血中での安定性を大幅に向上させた改良型核酸技術。この技術により、アンチセンス核酸薬(特定の遺伝子発現を抑制する薬)やmiRNA阻害薬の効果を高めることができる。神経疾患、がん、骨疾患、皮膚疾患、眼疾患など幅広い疾患領域において、アンチセンス核酸薬の研究開発や、タンパク質を作らない遺伝子(非コードRNA)の機能解析研究で広く活用されている。
これらのキーワードから、アンチセンス核酸やmiRNA制御、人工核酸修飾といった遺伝子のはたらきを抑制する技術の多様化と、核酸医薬の厳格な品質基準(GMP)に適合した製造および大量生産への対応という方向に研究投資がおこなわれていることが示されており、がん、神経疾患、感染症など従来の治療法では効果が限定的な疾患への核酸DDSの実用化にむけた研究資金配分が活発化していることがわかります。
以下に注目のグラント事例を紹介します。
- Biology and Targeting of noncoding RNAs in AML(急性骨髄性白血病における非コードRNAの生物学と標的治療)
- 配賦機関:NATIONAL CANCER INSTITUTE
- 期間:2023~2026年
- 研究機関名:UNIVERSITY OF UTAH(アメリカ)
- 概要:染色体異常のない急性骨髄性白血病でもっとも多くみられるNPM1遺伝子変異をもつ患者において、異常に多く発現している長鎖非コードRNA「HOXB-AS3」の病気への関与をあきらかにし、治療への応用をめざす研究。HOXB-AS3は細胞内のEBP1というタンパク質と結合し、細胞内でタンパク質を作る装置(リボソーム)の機能を調節し、白血病細胞の増殖を促進することがわかっている。このプロジェクトでは、そのくわしい仕組みを特定するとともに、改良型核酸薬(LNAギャップマー)をナノ粒子につつんだ標的治療薬の効果と安全性を検証し、治療が困難な急性骨髄性白血病(AML)のあたらしい治療戦略の確立をめざしている。
- Elucidation of mechanism of deterioration of multiple sclerosis mediated by connexin 43 binding microRNA and development of treatment(コネキシン43結合マイクロRNAが媒介する多発性硬化症の病態悪化メカニズムの解明と治療法の開発)
- 配賦機関:独立行政法人日本学術振興会
- 期間:2024~2027年
- 研究機関名:九州大学(日本)、国際医療福祉大学(日本)
- 概要:細胞が分泌する小さなカプセル(エクソソーム)が血液脳関門を通過できる特性に注目し、多発性硬化症(MS)において特定のタンパク質(GJA1-29k)をもつエクソソームと、炎症をひきおこすmiRNAが病気の悪化にどう関わっているかを解明する研究。(1)患者の血液と髄液中のmiRNA(Cx43結合miRNA)と病気の重症度の関係を調べ、(2)培養した免疫細胞などをもちいてそのmiRNAがどのように病気を悪化させるかのしくみをあきらかにし、(3)病気を再現した実験動物でmiRNA阻害薬(アンタゴミル)による治療効果の検証により、MSのあたらしい診断方法と治療法の確立をめざす。
つづいて、グラントの件数および配賦額(均等割)を見ます。核酸DDSに関連するグラントの国別件数推移が図6、配賦額の推移が図7です。中国はグラントデータの開示状況が年により大きく異なり、実態を反映しない可能性が高いことから除外しています。また、公開直後のグラント情報はデータベースに格納されていない場合があり、直近の集計値については過小評価されている可能性があります。
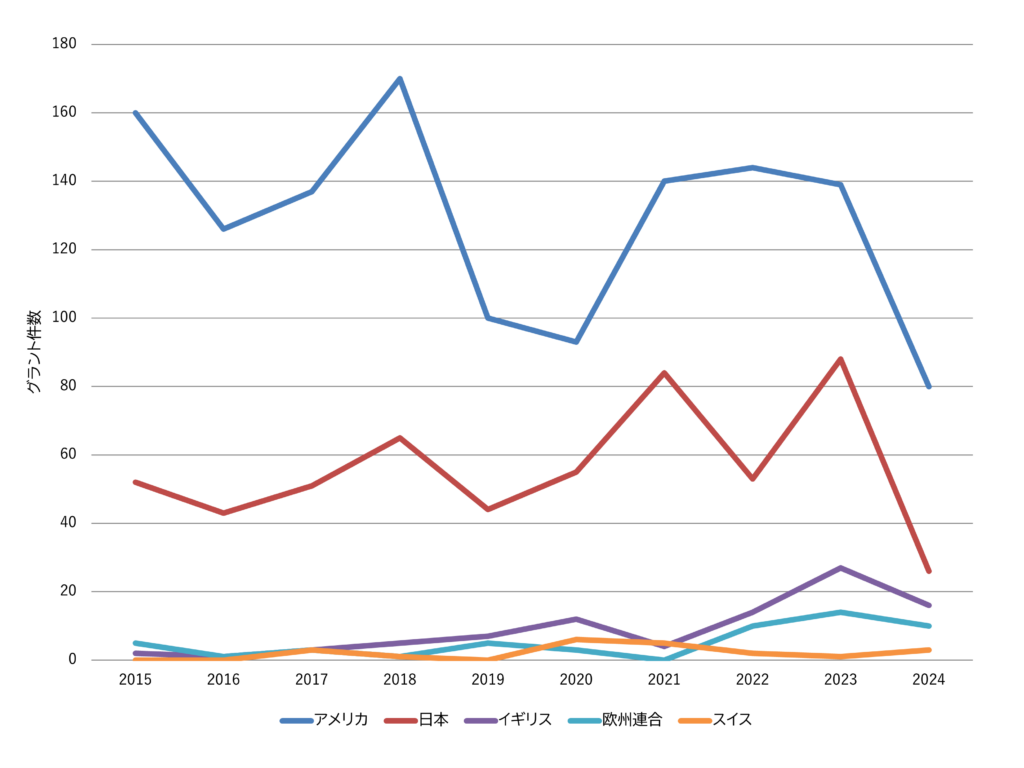
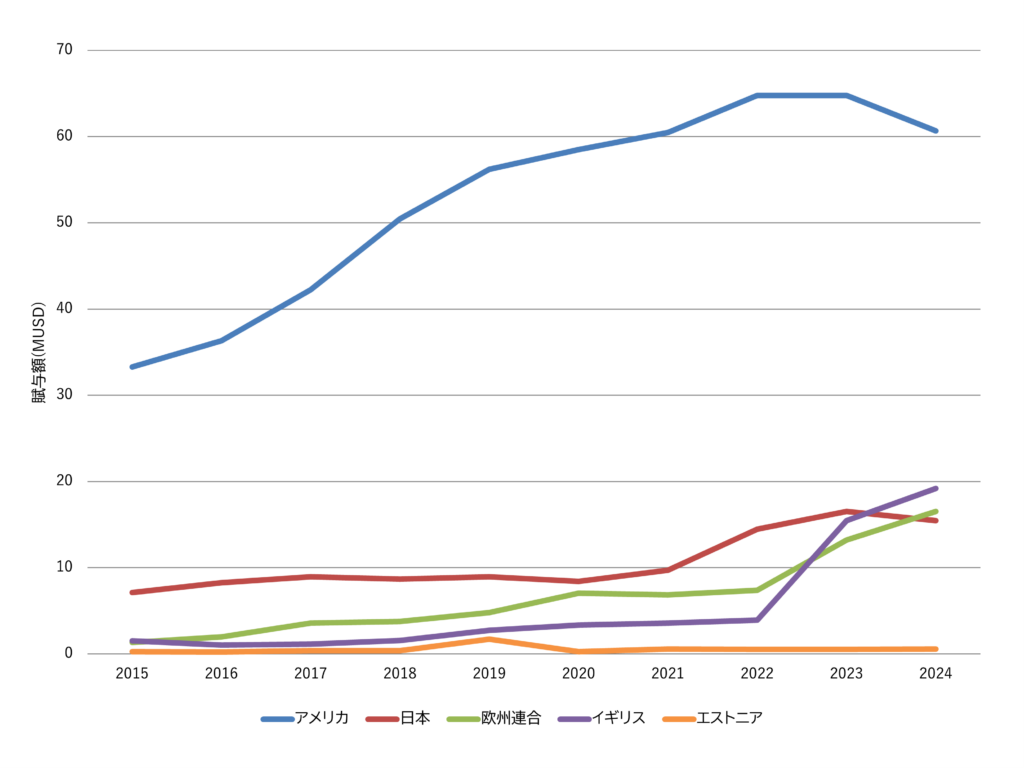
グラントの件数ではアメリカが最多ですが、日本も一定数が確認されます。賦与額はアメリカが圧倒的に多く、日本なども増加傾向にあります。日本のグラント数については、日本学術振興会や日本医療研究開発機構(AMED)などによる支援が継続されていることが要因です。
アメリカでは国立衛生研究所(NIH)傘下の各機関を中心に、がんや感染症、循環器や肺疾患分野の核酸DDS研究に資金が投入されており、肝臓以外の組織への送達拡大やmRNA、siRNA、ASOの臨床移行を目的としたLNP技術開発も重視されています。とくに国立がん研究所はRNA Biology Initiative Workshop「RNA Therapeutics」を2024年に開催し、治療用オリゴヌクレオチド、送達技術、RNA標的低分子、前臨床開発の加速が試みられています。
日本では、 日本学術振興会と日本医療研究開発機構を中心に、中枢神経疾患への全身投与をめざす血液脳関門通過型のヘテロ2本鎖核酸の開発プロジェクト、細胞内での薬の放出効率の抜本的改善をねらった特殊な脂質(環状ジスルフィド含有脂質)を組みこんだLNP(脂質ナノ粒子)の研究、肝臓以外の臓器への核酸送達における「第二のGalNAc」(肝臓への送達に成功したGalNAc技術に続く画期的な送達技術)の創出をめざす次世代送達技術プロジェクトなどが行われています。
EUでは、脳への治療用RNA送達による治療を目指すB-SMARTプロジェクト、設計段階から品質を作りこみ、厳格な医薬品製造基準に適合したmRNA送達ナノ医薬プラットフォーム構築をめざすEXPERTプロジェクト、LNP(脂質ナノ粒子)にかわる体内で自然分解されるペプチド担体による肝臓以外の組織へのRNA送達を開発するTraffikGene-Txプロジェクトなど、LNP製造基盤の高度化と肝臓以外への送達の実現にむけた研究投資が活発化しています。
核酸DDSに関連するスタートアップ企業の事例
核酸DDS分野では、多数のスタートアップ企業が革新的な技術開発と積極的な資金調達を展開しています。以下に、近年注目される主要スタートアップ企業を紹介します。
- ReCode Therapeutics
- 所在国/創業年:アメリカ/2015年
- 事業概要:mRNAおよび遺伝子修正医薬品を開発するジェネティックメディシン企業。SORT脂質ナノ粒子(LNP)技術をもちいて、従来困難とされてきた肝臓以外の臓器や細胞への精密な核酸送達を実現し、遺伝性疾患の治療薬開発を推進する。
- 技術特徴:SORT-LNP技術により、肺や骨髄など肝臓以外の組織への選択的臓器ターゲティングを実現。mRNAと遺伝子修正の双方に適用可能な汎用性を持つ。
- 20Med Therapeutics
- 所在国/創業年:オランダ/2011年
- 事業概要:siRNA・miRNA(遺伝子発現を調整する核酸医薬)の標的送達に特化した、ポリマー系ナノゲル(合成樹脂でできた超微細なゲル状粒子)を開発するオランダのバイオ企業。遺伝性疾患の治療を対象に、核酸DDSにおける薬の安定性、細胞への毒性、細胞内での薬の放出といった根本的な課題の解決に取りくむ。
- 技術特徴:ポリマーハイブリッドナノゲル(20Med-nanogel)は粉末状態での長期保存が可能で、水に溶かして核酸を簡単に組みこむことができ、細胞内の薬の放出機能を化学的に組みこむことで、薬が細胞質に効率よく到達できるしくみを実現する。
- SiSaf
- 所在国/創業年:イギリス/2008年
- 事業概要:RNAデリバリーおよびRNA治療薬を開発するバイオ企業。独自のBio-Courier技術をコアとして、希少遺伝性疾患むけRNA医薬品パイプラインを構築するとともに、技術ライセンスおよび研究パートナーシップを展開する。
- 技術特徴:Bio-Courier技術は、有機脂質と無機の体内吸収性シリコンをくみあわせたシリコン安定化ハイブリッドLNP(sshLNP)により、従来のLNP(脂質ナノ粒子)と比較してRNAの安定性と安全性、遺伝子導入効率を向上させる。
- TriPhos Therapeutics
- 所在国/創業年:アメリカ/2010年
- 事業概要:RNAi治療薬企業向けにsiRNA送達技術を提供する企業。siRNAプラットフォーム(遺伝子発現抑制薬の基盤技術)の標的化能力向上と、特殊な化学保護基をもちいた治療用核酸の合成技術の開発を主軸とする。
- 技術特徴:siRNA送達に特化した化学保護技術を採用し、より特定の表的に正確に作用し、効果の高いRNAi治療薬の製造を可能にする核酸合成技術を有する。
- Tinker Therapeutics
- 所在国/創業年:アメリカ/2024年
- 事業概要:神経変性疾患などを対象に、複数の標的に同時に作用するオリゴヌクレオチド治療薬(短い核酸医薬)を開発。
- 技術特徴:FORGEプラットフォームにより、ASO・siRNA(遺伝子発現抑制薬)を2個、3個、あるいは4個つなげた多量体構造に改良。独自の化学修飾パターンと薬剤設計により、脳全体への薬の分布と持続的な遺伝子発現抑制を実現し、複数の遺伝子を同時に制御することを単一の薬剤分子で達成する。
- Norn Gene
- 所在国/創業年:中国/2011年
- 事業概要:核酸医薬送達と配列修飾技術を専門とする中国のバイオ企業。独自LNP+プラットフォーム(改良型脂質ナノ粒子技術)による生体内核酸デリバリーを中核事業とし、次世代mRNA医薬品の有効性・安全性向上をめざした統合技術基盤を構築する。
- 技術特徴:LNP+プラットフォーム(改良型脂質ナノ粒子技術)に加え、DNA/mRNA配列にタンパク質発現量の増強と発現時間の延長を促進する要素(エンハンサー)のくみこみ技術を独自開発し、両技術を統合した独自の知的財産権を保有する。
- Capstan Therapeutics(AbbVie社によって2025年買収)
- 所在国/創業年:アメリカ/2021年
- 事業概要:主要な候補薬であるCPTX2309が自己免疫疾患を対象にPhase 1試験(第1相臨床試験:人での安全性を初めて確認する段階)中の企業。
- 技術特徴:抗体などのタンパク質を結合した標的化LNP(CellSeeker tLNP:特定の細胞を狙う脂質ナノ粒子)で、体外での細胞操作なしにキメラ抗原受容体T細胞(CAR-T細胞)等を生体内で直接リプログラミング。
これらのスタートアップ企業は、特定の臓器を狙い撃ちするLNP(脂質ナノ粒子)、核酸医薬の化学修飾や複数の分子をつなげる技術など多様なアプローチで核酸DDS技術を開発しています。肝臓以外の臓器への標的化拡張と細胞内での薬の放出効率の改善への取り組みも活発です。
薬を運ぶLNP(脂質ナノ粒子)の研究開発のみならず、あたらしい核酸医薬の開発も進められており、それらの研究成果が相互に作用し合うことで核酸DDSの実用性が向上することが期待されます。また、すでに臨床試験が実施されている技術もあり、核酸DDSの社会実装が着実に進展していると考えられます。
核酸DDSに関連する技術動向のまとめ
本レポートでは、核酸DDSに関連する特許、論文、グラント、及びスタートアップ企業のデータベースにもとづいて年次推移の解析をおこない、技術動向を分析しました。
特許分析からは、実用化段階に向けた技術の成熟が顕著に読み取れます。特に「lipidoid(脂質様物質:従来の脂質を改良した薬物運搬材料)」「sa-mRNA(自己増幅型mRNA:細胞内で自分自身をコピーして増殖できるmRNA)」「GalNAc-siRNA(N-アセチルガラクトサミン修飾siRNA:肝臓に選択的に届くsiRNA)」といったキーワードの成長は、核酸をつつんで運ぶ技術の多様化、少ない投与量でより長期間効果を発現させる応用拡大、特定の組織を狙ったsiRNA送達の実用化が進展していることを示しています。
論文分析からは、製剤設計・塩基修飾・担体製造法・生体由来担体に関する技術の発展が研究の主要トレンドとして浮上していることがわかります。「PEG-lipids(ポリエチレングリコール結合脂質:脂質ナノ粒子の表面を改良する成分)」「nucleoside-modified(修飾ヌクレオシド:免疫反応を避けながらタンパク質産生効率を向上させる技術)」に示される運搬材料や核酸の改良技術や、「microfluidic(マイクロ流体:微細流路を使った精密製造技術)」に示される製造技術の革新は、核酸DDSの実用性を飛躍的に拡大する可能性を秘めています。また、中国やアメリカがこの分野の技術進歩を率いていることも示されました。
グラント分析からは、遺伝子の働きを抑制する技術の多様化と、核酸医薬の臨床応用に向けた研究投資が確認されます。「gapmer(ヌクレアーゼ耐性アンチセンス核酸:体内の分解酵素に強い遺伝子発現抑制薬)」「LNA(Locked Nucleic Acid:標的への結合力と血中安定性を向上させた改良型核酸技術)」をふくむ研究への資金配分は、従来の核酸DDSがかかえる技術的課題の克服への研究投資が活発化していることを示しています。また、そうして得られた研究成果の社会実装を、「Good Manufacturing –Practice(製造管理及び品質管理の基準:医薬品の厳格な製造基準)」「scalable(大規模に実現可能:実験室レベルから大量生産まで段階的に拡大できる技術)」をふくむ研究開発によってめざす動きも見てとれます。
核酸DDS市場では、世界的なヘルスケア企業であるMerck & Co.がModerna社と共同研究をおこない、その核酸DDS技術を応用するなど、ダイナミックな企業間のコラボレーションが見てとれます。その中でスタートアップ企業は、特定の臓器を狙い撃ちするLNP(脂質ナノ粒子)、核酸医薬の化学修飾や複数の分子をつなげる技術など多様なアプローチで核酸DDS技術を開発しており、大手製薬会社との共同やM&A(企業買収・合併)によって、ますます技術革新が促進されていくものと考えられます。
今回の分析では、従来の核酸DDSのかかえていた体内での安定性などの課題の解決や、適切な組織の狙い撃ちによる副作用の軽減、標的への結合力や細胞内での薬の動きの改善による薬効の増大のための研究が加速していることが確認されました。また、それらの研究成果の社会実装が製造面などの充実によって積極的に推進されていることも分かりました。
感染症や難病に対する医療ニーズの高まりにより、遺伝子発現レベルでの精密な治療を可能にする核酸DDSへの需要は今後ますます拡大していくと考えられます。がん、神経・筋疾患、遺伝性希少疾患などの分野で、核酸DDSを基盤とした医薬品の社会実装が今後も進展していくと考えられます。
著者:アスタミューゼ株式会社 平澤 輝一 博士(理学)
さらなる分析は……
アスタミューゼでは「核酸DDS」に関する技術に限らず、様々な先端技術/先進領域における分析を日々おこない、さまざまな企業や投資家にご提供しております。
本レポートでは分析結果の一部を公表しました。分析にもちいるデータソースとしては、最新の政府動向から先端的な研究動向を掴むための各国の研究開発グラントデータをはじめ、最新のビジネスモデルを把握するためのスタートアップ/ベンチャーデータ、そういった最新トレンドを裏付けるための特許/論文データなどがあります。
それら分析結果にもとづき、さまざまな時間軸とプレイヤーの視点から俯瞰的・複合的に組合せて深掘った分析をすることで、R&D戦略、M&A戦略、事業戦略を構築するために必要な、精度の高い中長期の将来予測や、それが自社にもたらす機会と脅威をバックキャストで把握する事が可能です。
また、各領域/テーマ単位で、技術単位や課題/価値単位の分析だけではなく、企業レベルでのプレイヤー分析、さらに具体的かつ現場で活用しやすいアウトプットとしてイノベータとしてのキーパーソン/Key Opinion Leader(KOL)をグローバルで分析・探索することも可能です。ご興味、関心を持っていただいたかたは、お問い合わせ下さい。